- [2018/3/12] 2018年亨汀頓氏症治療研討會-第三天會議摘要
-
更新亨汀頓氏症治療研討會第三天會議內容:huntingtin蛋白質 – 以及如何將其降低!
由Dr. Jeff Carroll於2018年3月2日撰寫,Dr. Ed Wild編輯。
今天是2018年亨汀頓氏症治療研討會的最後一天,今天有兩個議題。首先聚焦在HD基因所生成的蛋白質,其次的是Wave Life公司與Ionis公司的huntingtin降低試驗的更新。週四上午議程 – huntingtin蛋白
每位HD患者遺傳了相同的變異 – C-A-G片段的延長。此延長位於我們稱為HD基因上。細胞利用基因來做為生產蛋白質的依據 – 今天第一個議程聚焦在HD蛋白。

Dr. Kochanek以HD基因發現二十五周年的蛋糕樣子展示了Huntingtin蛋白的結構式。來自格勒諾布爾大學(Universite Grenoble Alpes)的Sandrine Humbert長期從事大腦發育的研究,以及HD基因跟蛋白是如何影響其過程。為了瞭解此過程,Humbert的實驗室培育了一種腦部缺乏HD基因與蛋白的小鼠。他們發現缺乏HD基因的細胞委以不正常的方式分裂以及運行。在腦部發育過程中,新生的細胞會沿著其他細胞所形成的”繩索”攀登到適當的位置。當HD基因被刪除時,這過程會受到影響。意味著HD在此過程中可能扮演重要的角色。
來自IRBM Science Park的Andrea Caricasole正進行一項跟Huntingtin蛋白有關的轉譯後修飾(post-translational modifications)的大型試驗。也就是跟huntingtin蛋白有關的微小化學修飾。這些修飾能調整蛋白質的功能。以Huntingtin蛋白為例,有數十種的標籤被加上或是移除,好調整huntingtin蛋白的功能以便對於不同訊息有所反應。這些修飾過程會對huntingtin蛋白進行許多有趣的作用,甚至能預防變異的huntingtin蛋白從受損的細胞中產生。之前有在HDBuzz的文章中提及。Caricasole的團隊正在開發對於個別huntingtin蛋白修飾作用的敏感性測試。這些測試能讓他們追蹤病程中有哪些被改變,或許能找到修正它們的方法。
來自華盛頓大學(Washington University)的Rohit Pappu聚焦於研究huntingtin蛋白。 他的實驗室正開發相關的工具,以了解受到HD突變而影響形狀的蛋白質部分。Pappu的實驗室運用電腦來嘗試預測受到突變影響形狀的huntingtin蛋白的形狀。這些技術能讓他們觀察這些”蝌蚪狀”(“tadpole” shape.)的形狀。這一種蝌蚪狀的形狀在HD領域中是個被激烈爭論的話題。Pappu的技術強烈的支持了這爭辯中的某一面,能幫助我們更了解huntingtin蛋白的關鍵之處。
來自埃默里大學 (Emory University) 的Xaio-Joang Li 開發了一個有趣的小鼠模型,在成年小鼠的腦部、身體或是兩者當中,可以關閉HD基因。這些小鼠並沒有延長的huntingtin基因 – 這能幫助我們了解如果把正常的基因關閉是否會有相關影響。令人欣慰的是,當關閉基因時,腦部並沒有負面的影響。令人意想不到的是,關閉基因後造成胰臟的發炎。尚不清楚對於患者有何意義,但是目前huntingtin降低療法並非傾向降低全身的huntingtin,而是僅針對腦部。Li同時利用CRISPR-Cas9基因編輯技術將小鼠的HD基因中有害部分剪除。讓小鼠的變異基因失去功能成功地減少了有毒的huntingtin蛋白,同時讓小鼠更好活動。Dr. Li同時也利用CRISPR基因編輯技術設計HD豬模式。這對於測試新藥物是相當有用的,因為豬的大腦跟人腦是相似的。
“Kochanek將huntingtin蛋白凍住並利用電子微束拍攝上千張的照片。之後利用電腦將其合成為首次清楚呈現huntingtin蛋白結構的照片(Kochanek froze the protein and used an electron beam to take thousands of photos of it. Those were then combined by computer to produce the first ever pictures of the detailed molecular structure of the huntingtin protein.)。”
來自聖地牙哥加州大學(UCSanDiego)的Ankur Jain 從事RNA的研究 – 這是一種當細胞想利用DNA中的指引生產蛋白質時,所產生的訊息分子。我們的DNA位於細胞核當中,而RNA則是飄散在整個細胞內。關於遺傳性腦部疾病的傳統觀點認為,疾病是由毒性蛋白所引起,但是隨著增加的證據顯示,從變異基因產生RNA訊息分子可能也具有毒性。例如,某些RNA序列會附著在重要的蛋白質並阻止其在細胞中的功能。關於毒性RNA的可能跡象是在HD與其他腦疾病中,細胞中被發現的異常RNA斑點(blobs of RNA)。Jain發現他可以像煮果凍一樣,先加熱再冷卻以形成人造的RNA斑點。 這些斑點僅會當RNA包含黏性序列時形成,像是HD中CAG的序列。尚不清楚這些RNA斑點是否造成HD的傷害,或許會。例如,如果RNA卡在細胞核,它就無法生成蛋白質。反義分子(Antisense molecules,類似近期HD人體試驗中的藥物)能附著 細胞核中的RNA,並阻止其生成斑點。其他藥物理論上也可用來解決腦部疾病中RNA黏性的問題。
下一個精彩的演講是由Stefan Kochanek進行,他的實驗室剛發現了huntingtin蛋白的結構! 發現蛋白質的構造形狀是非常重要的步驟,因為可藉此了解它們是如何運作以及如何利用藥物來改變。Huntingtin基因是25年前被發現的,但是因為構造太大、易搖擺又具黏性,因此很難探究其結構。有個團隊甚至將其射向太空以期獲得結晶,但是失敗了。Kochanek的團隊在其他人失敗的地方成功了,並在近期發表於Nature期刊。最大的突破點在於利用一種稱為HAP40 (“huntingtin-associated protein 40”)的蛋白質,來將huntingtin穩定住。一旦藉由HAP40穩定之後,Kochanek將huntingtin蛋白凍住並利用電子微束拍攝上千張的照片。之後利用電腦將其合成為首次清楚呈現huntingtin蛋白結構的照片。這真的是很棒的結果同時給予我們許多後續進行的研究。需要注意的是 – 某些區域仍不穩定無法顯示出結構 – 例如很重要的包含著變異處的蛋白質前端。
週四下午議程 – 降低huntingtin
今日大會以Huntingtin降低療法的議程作為結尾。Huntingtin降低(Huntingtin lowering)意指著將huntingtin蛋白降低的方法。有許多方式可達到這目的,但大多是針對RNA來進行,因為RNA是HD基因訊息與huntingtin蛋白的中介者。
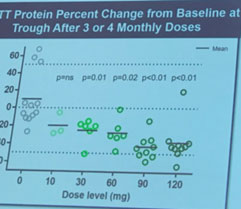
這是一張很重要的圖片! 它顯示了腦脊髓液中,不同劑量的HTTRx降低的變異huntingtin比例 – 較高的劑量可降低近50%,這是很棒的結果。來自柏克萊大學(UC Berkeley)的Michael Rape從事誘導細胞來摧毀細胞中個別蛋白質的研究。在許多例子中,包括HD,如果能選擇性的移除某些特定蛋白質是非常有幫助的。細胞有著多種將蛋白質降解的機轉 – 其中之一就是利用一種被稱為泛素(ubiquitin)微小蛋白來進行化學標示的方法。細胞會把泛素視為”請吞噬”的訊息,並將帶有此標示的蛋白分解破壞。Rape的實驗室一直從事於研究細胞是如何運用泛素作為標籤,快速的將被標示的蛋白質破壞 – 例如有毒的蛋白。Rape的實驗室已經建立了工具,能讓研究人員首次觀察蛋白質如何經歷這種快速破壞途徑。快速的蛋白質破壞途徑是個有用的工具 – 同時也是Rape實驗室專注的操控方式。近期一個被稱為PROTAC的技術 – 能讓研究者操控泛素系統來指引細胞摧毀特定蛋白。
來自維吉尼亞大學(University of Virginia)的Scott Zeitlin從事於利用HD小鼠來研究,當我們降低正常huntingtin、變異huntingtin或是兩者都降低之後會發生何種結果。請記住每一個人會從父母各自遺傳一個huntingtin – 多數的人會獲得一個正常以及一個異常的複製。科學家將健康/正常蛋白質稱為”野生型(wild-type)”,因為它是比較常見的型態。這些問題很重要是因為所有的huntingtin降低療法,都是聚焦在把腦中的huntingtin數量全部降低。某些方法,像是Ionis的藥物,會平均的將兩種蛋白質降低。其他的方式,例如Wave的藥物,嘗試將變異蛋白降的比野生型更低。我們認為將變異蛋白單獨降低或至少跟野生型同樣是比較有益的 – 但是降低huntingtin是否安全仍是個沒有答案的疑問。Zeitlin培育了能產生變異的、野生型或是兩者蛋白質的小鼠,並在其成長後被減少的小鼠品種。Zeitlin發現於早期降低變異huntingtin,對於減少腦中蛋白堆積有較大的成效。同樣的,早期的降低變異huntingtin對於體重流失或是動作技巧有較好幫助。同時減少兩種蛋白質同樣有好處 – 早期治療具有較大的益處。
當抑制huntingtin時,越早治療越好。進行抓握力試驗時,僅降低變異蛋白質有顯著改善,但是同時降低兩種蛋白質則沒有。大致而言兩種方式都是有幫助的,關鍵點在於多早給予治療。Zeitlin同時研究當再度給予huntingtin時會發生甚麼事情,發現對試驗的小鼠而言會有不良影響。這意味著長期治療會比短期治療好 – 如同我們所預期的一樣。
來自奧勒岡健康與科學大學(OHSU)的Jodi McBride說明她的研究,利用一種無害的病毒將指示送到腦部細胞,讓它們自己生產破壞RNA的分子。這方式的好處之一就是病毒能讓RNA破壞分子持續生成,理論上是種一次性治療。McBride在猴子身上進行這項研究,猴子具有較大、複雜且與人腦類似的大腦。特別的是,她的團隊從事於將病毒送到腦中被稱為殼核部位(putamen)的研究。殼核特別的有趣,因為它是HD中最脆弱的腦部區域之一。 - 在遺傳到HD突變的人們當中,殼核會大量的萎縮。McBride描述了為了傳送病毒,腦部手術所需要的改進,包括利在注射時用MRI顯示腦部影像。 病毒的治療能減少殼核中大概一半的帶有HD基因RNA,這是以前就嘗試達到的改善。下一位是來自Wave Life Sciences公司的Mike Panzara,他規劃了兩個利用反義寡核苷酸(Antisense Oligonucleotides, ASOs)進行針對HD的臨床試驗。ASOs是能進入細胞摧毀目標RNA,減少目標蛋白質濃度的一種短小、經修改的DNA。
Panzara告訴觀眾目前Wave公司正針對HD患者進行兩個有關ASOs的臨床試驗。為何進行兩個?Wave 的方法依賴著瞄準HD基因中微小的基因變異 – 稱為SNPs或是snips。這些微小的變化不會造成HD,他們只是人與人之間正常遺傳變異的一部分 – 這也是我們不是同卵雙生的原因。有趣的是,這些變異僅於每個人都有的兩套複製的HD基因中的其中一套被發現。藉由瞄準這些變異,Wave公司的ASOs能分辨HD基因中突變與非突變的複製。Wave公司正進行兩個ASOs試驗早期的安全性試驗,分別是PRECISION-HD1以及PRECISION-HD2。 ASOs被用於針對HD基因中基因變異的部分。此方法的秘訣在於人體不僅需要繼承HD的突變,同時必須伴隨著會讓突變的基因複製獨特性標靶的變異(The trick with this approach is that people not only have to have inherited the HD mutation, but accompanying variants that allow the mutant copy of the gene to be uniquely targeted.)。因此這些試驗必須聚焦於帶有這些變異的患者。Wave公司已經發展相當酷的新技術來檢測這些變異,以及確定這些變異是在HD的突變複製上,而非位於正常的複製。 Wave公司進行了一項初步的研究,這研究中他們能在64%的自願者身上發現ASOs的目標。
“Tabrizi對於第一個試驗的勇敢自願者鼓掌,並稱之為真正的研究英雄。”(Spontaneous applause as Tabrizi thanks the brave volunteers in the first study, calling them “true research heroes”.)
接下來,來自Ionis公司的Anne Smith以及倫敦大學學院(UCL)的Sarah Tabrizi報告了一個關於ASOs針對HD基因兩套複製的臨床試驗。這是一個多年研究的累積 – Smith提醒聽眾,Ionis的計畫是從2005年開始的! 他們起始於細胞以及動物研究,對於ASO的療法能減少huntingtin蛋白質、改善類HD症狀提供了初步的證據,。在2012與2013所發表的結果,HD小鼠模型的研究中顯示huntingtin的降低能改善類HD症狀。Smith概述Ionis藥廠選擇ASO來針對HD基因兩套複製而非針對突變的複製的邏輯。ASOs的好處之一就是它們廣布於腦中。Smith展示了猴子試驗中的資料,顯示注射到脊髓液中之後,ASOs廣布於腦中。Ionis公司也研究了在較大動物身上的散布情況,例如在豬的身上,發現同樣廣布於腦中。 之後進行了毒性測試,顯示長期使用下藥物是具有良好耐受性的(在猴子身上長達15個月的研究)。因為不太可能從接受ASOs治療的患者身上取得腦部樣本 – 我們該如何知道ASO有發揮效果呢?Smith描述了猴子的試驗建立了腦部huntingtin降低與脊髓液中的降低的關聯性。這讓Ionis公司能建立一個非常複雜的電腦模型,藉由腰椎穿刺以預測在腦部與脊髓液會有多少Huntingtin降低。此時Ionis公司跟另一個製藥業夥伴,Roche公司一起合作,來進行ASOs的人體試驗。
Sarah Tabrizi 介紹了由Ionis / Roche所進行的第一個ASO人體試驗。此試驗是個安全性研究 – 研究的目的是了解藥物是否安全。試驗進行於英國、德國以及加拿大的九個中心。從脊髓液注入ASOs,以緩慢調升(亦即受試者一開始接受較低的劑量,之後慢慢增加劑量)的方式進行。如此謹慎的增加劑量方式,主要是使獨立於試驗的醫師來評估藥物的安全性。此試驗招募了46位勇敢的自願者,他們願意冒著風險來當第一批接受此藥物治療的受試者。研究者能測量脊髓液中huntingtin蛋白的濃度 – 在此之前無法跟腦部的濃度獲得良好的比例關係。(需記住,我們無法直接測量腦部資料)。
降低的幅度是相當驚人的 – 平均下降了40~50%! Tabrizi描述了研究人員的感覺,huntingtin降低的效果至少可持續六個月。 以下是Tabrizi所預測,腦部蛋白降低的相對應量。Ionis公司已建立一個模型,讓他們能預測脊髓液與腦部huntingtin降低的關聯性。顯示著大量降低了腦組織中的huntingtin。受試者被謹慎的監測其安全性,沒有重大不良影響被發現。Tabrizi表示 – 藥物在測試的各劑量範圍是安全且耐受性良好。試驗成功了! 參與試驗的全體受試者正在進行所謂的開放性標籤延展試驗(open label extension) – 原先接受安慰劑的受試者都接受藥物治療並被觀察著。Tabrizi鼓掌並感謝第一個試驗中的勇敢自願者,稱呼他們為真正的研究英雄。
會議最後以Roche以及Ionis公司正在規畫下一次試驗的時間做為一個讓人興奮的結尾,它們將進行的是更大規模、研究此藥物是否能改善HD症狀的人體試驗。
|


