- [2018/9/17] 羅氏製藥(Roche)宣布關於其具關鍵性的降低huntingtin的研究細節
-
GENERATION-HD1 試驗將測試RG6042 – 先前名稱為Ionis-HTTRx – 是否能延緩HD(Huntington's disease,亨汀頓舞蹈症)的病程
由Jeff Carroll博士於2018/9/17撰寫,Ed Wild博士編輯,Charles Yang翻譯
現下是huntingin降低藥物研發的重大發展時期,目標是降低會造成HD的huntingin蛋白。在上週舉辦的歐洲亨汀頓舞蹈症網絡會議( European Huntington’s Disease Network, EHDN)當中,Roche宣布了關於降低huntingtin 藥物,RG6042第一個關鍵性研究的細節 - 或者你較熟悉的名稱為Ionis-HTTRx。讓我們來看看這試驗的相關細節。
何謂降低huntingtin?
首先,先簡單回顧一下治療HD中,降低huntingtin此方法。請記得,HD病程中是,造成腦部傷害的毒性蛋白質被稱為突變huntingtin。HD的基因 – 有時也被稱為huntingtin基因 – 是用來製作huntingtin蛋白的設計圖。

Scott Schobel在維也納舉辦的EHDN當中宣布關於GENERATION-HD1的設計。當某個細胞需要更多的特定蛋白質,例如說huntingtin蛋白,它會製作一些基因的臨時備份 – 一種由稍微不同的化學物質編寫的訊息分子,稱為RNA。因為這個RNA帶有一段訊息,科學家稱為訊息RNA (messenger RNA)或是mRNA。從基因到訊息攜帶者到蛋白的傳遞過程中,如果有任何的破壞,細胞就不會製作任何此特定蛋白。
這就是huntingtin降低方法用以治療HD的方式 – 藉由瞄準huntingtin訊息RNA 並告知細胞來忽略或是刪除此RNA。越少的訊息,就產生越少的蛋白質。
Most HD researchers find this approach very exciting, because common sense and a ton of animal research suggests that if you reduce or eliminate the mutant huntingtin protein, you lessen the severity of HD symptoms.
反義寡核甘酸(antisense oligonucleotides, ASOs)在HD的研究
早期在huntingtin降低的領域中,在加州Carlsbad的Ionis生技公司是領頭羊。在過去十幾年間,該公司發展了一種被稱為反義寡核甘酸(antisense oligonucleotides, ASOs)的技術,也就是一種被修改的DNA – 就如同被摺疊於細胞中,被設計來辨識特定訊息RNA的分子。
當這些ASOs附著到被設計來辨識的目標當中,細胞會摧毀它,大幅度降低此特定的訊息RNA。較少的訊息者代表較少的蛋白質會被生成,即使HD基因仍存在DNA中。
基於動物測試的成功,Ionis在2015年進行了針對46位勇敢的HD患者的起始試驗。這個小型試驗僅被設計來了解被稱為HTTRx的藥物是否安全,以及以HTTRx治療是能減少神經系統中的huntingtin蛋白。我們無法取得腦部細胞樣本,但是我們能從大腦浸泡著的脊髓液中測量變異huntingtin蛋白的濃度。
如同在HDBuzz討論過的,於2017年12月時,Ionis與他們的夥伴,Roche宣布此試驗成功了。值得注意的是,46位參加者中沒有任何一人脫離試驗,儘管每個月都需要從脊髓注射試驗藥物。而更加值得關注的是,以HTTRx治療明顯地降低了脊髓液中huntingtin蛋白的濃度。
Roche是一家位於瑞士的大型製藥公司,在美國的分支稱為Genentech。除了第一次試驗的好消息之外,Roche確認它將會計劃、主導下一個HTTRx的試驗,而在移交之後HTTRx被更名為RG6042。 之後請習慣RG6042此名稱 – 也請記得這個就是我們一直在討論的HTTRx同樣藥物。
用此測試效果的試驗
無庸置疑的,研究者以及HD社群有興趣的是如何延緩HD病程,而非改變脊髓液中測量到的濃度改變。但是Ionis的成功安全性試驗僅針對46位受試者進行三個月研究而已 – 試驗太短而且規模太小,無法顯示治療對於HD症狀是否有任何影響。
“GENERATION-HD1試驗將會在2018年年底開始,2019年年初預計收錄第一位患者。它將會在15個國家中的80到90個研究中心進行試驗。 (GENERATION-HD1 will launch at the end of 2018, with the first patients enrolled in the beginning of 2019. It will take place at around 80-90 sites in about 15 countries. )”
現在我們知道Ionis/Roche的藥物可以降低蛋白質,看起來是安全的,接下來我們需要的是一個針對更多受試者的大型試驗 – 也就是第三期臨床試驗(phase 3 trial) – 來了解RG6042是否能減緩HD病程。
從去年12月我們就非常期待此一大型臨床試驗的宣布。而在今年9月16日,我們等到消息了!
GENERATION-HD1試驗
在2018年的EHDN會議中,Roche的Scott Schobel提供了即將到來的試驗的第一次官方簡介。試驗名稱稱為 GENERATION-HD1。
(GENERATION-HD1的名稱來自以下名稱的縮寫: Global EvaluatioN of Efficacy and safety of Roche/genentech AnTIsense OligoNucleotide for Huntington’s Disease)
試驗規模很重要
GENERATION-HD1試驗將會在2018年年底開始,2019年年初預計收錄第一位患者。它將會在15個國家中的80到90個研究中心進行試驗。
目前尚無公布某個特別的研究中心,意味著尚無公開資訊得以了解試驗中心或是由哪個國家主導。希望能盡快有更多資訊揭露出來。
這是個很大型的試驗 – 預計招募有HD表徵(Manifest HD)的660位受試者。‘Manifest HD’ 表示受試者被正式診斷出有HD的臨床表徵,試驗將不招募有突變基因而未有臨床表徵的HD患者(premanifest 或是prodromal HD).
符合的資格(Eligibility)
有兩個臨床決定因素,或是又稱招募標準。第一個,受試者必須動態(ambulatory)以及言語(verbal) – 亦即能夠走動與說話。其次,必須在獨立的功能評估(Functional Assessment)的測試中獲得70分或是以上的分數。也就是針對日常功能的能力,像是能自己洗衣服、進行有限度的家庭活動,例如烹飪或是使用刀具。
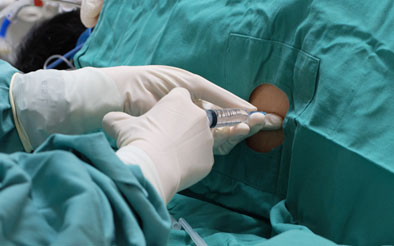
試驗將進行25次的脊髓注射,對於自願受試者而言是艱困的工作,三分之一個受試者會接受安慰劑的注射。這些招募標準比前一個試驗還寬鬆,前一個試驗嚴格限制在早期HD或是接近正常的日常功能。
另外有一個特別的評分要求,被稱為CAP分數的測試需要高於某個標準。
CAP分數是簡單的數學方式,結合了受試者的年齡以及他們的CAG數目 – 也就是導致HD的 DNA片段中異常的延長片段。會使用此分數主要是有些人具有較嚴重的HD變異(也就是較長的CAG片段),會在較年輕的時候就發病。因此如果我們想要追蹤某個人的HD症狀的病程,我們必須計算此人的年齡與CAG片段。設定一個最小的CAP分數標準,意味著此試驗可以聚焦在得以從試驗中獲得益處的患者,讓試驗可以在最小的規模,獲得最快的結果。
多次脊髓穿刺 (Lots of lumbar punctures)
此試驗將包括安慰劑組,大約有三分之一受試者被分配到此組。安慰劑組是必要的,用以對抗安慰劑效應 – 也就是參加試驗會讓受試者覺得症狀真的有改善,身體功能有增加,即使藥物並未發揮效果。
其他三分之二的受試者將會分成兩組,都會接受有效藥物測試。一半的治療組會每個月接受藥物,另一半則是兩個月一次接受有效藥物。這是很棒的設計,可以讓我們了解是否能以較少的給藥頻率,獲得相等的效果。但是每一組的受試者都是每個月接受脊髓注射,持續兩年。安慰劑組將會每個月接受安慰劑注射。每個月藥物的組別會每個月獲得藥物注射。兩個月接受一次藥物的組別,會每個月輪流注射藥物、安慰劑。也就是沒有人會知道他們會被分在哪一組。
底線:每一位受試者必須可接受多次的脊髓注射,也就是兩年內接受二十四次注射。
評估結果
試驗成功或是失敗,在美國由被稱為整體功能儲備量評分(total functional capacity scale, TFC scale)來決定。這是個很簡單的評分系統,依據每個人自行進行家庭事務、照顧自己的能力來評分。
在歐洲,試驗將由更精密的測量方式評估,該方式稱為綜合性統一HD評分表( composite Unified Huntington’s Disease Rating Scale , cUHDRS)。此評分計算更廣泛的HD症狀,結合了TFC評分,一個動作評分以及一些思考測驗。
“它將會是個非常大型的試驗 – 招募了660位有HD表徵的受試者 (It will be a very large study – enrolling 660 patients with manifest HD. )”
在不同國家以不同的設定終點進行研究,有些不尋常但也並非前所未聞。但是這些評分都是用以測量相同的進程,而進程會隨著HD病程逐漸變差,不同機構對於何謂最佳的測量似乎也有不同看法。最終,如果藥物有作用,我們可預期兩套評估方法都會朝向相同的方向前進。
並非所有受試者在試驗第一天就參與,因此這二十五個月的受試期間或許會延長兩倍,甚至更久的時間。
稍待一下,還有更多資訊
羅氏製藥同時也宣布了另一個研究 – 稱為Natural History Study,目的是藉此提供HD病程的關鍵訊息。預計招募100名受試者,並與進行中的RG6042開放性試驗來配對。這些開放性試驗的參與者是從第一個臨床試驗招募而來,目前正在規律性的服用藥物,因此natural history study可幫助我們了解開放性試驗產生的數據。如果這一切都按照計畫進行,Natural History Study的受試者,也將會在15個月的參與(包括數次的腰椎穿刺)後,接受開放性試驗的治療
還有更多的訊息!
在EHDN會議中,還包含了其他令人振奮的huntingtin降低計畫的訊息,像是Wave Life Sciences,PTC Therapeutics以及Uniqure等公司的計畫。我們將會陸續介紹EHDN 2018中相關資訊。
接下來呢?
緊接在第一個試驗顯示短期的安全性,以及成功降低huntingtin之後,我們現在有關鍵性試驗來了解RG6042是否有效,以及非常明確的時程表。
請謹記在心,參與GENERATION-HD1的試驗者,將面對漫長具有挑戰性的長路,參與其中是一項艱鉅的身心挑戰。
不可避免的,有許多人們因為任何一項原因而無法參與其中。對這些人而言會相當的失望,但是請記住,藥物將由來自全球的自願者測試,而這些試驗是為了每一個人以及下一代來測試藥物,並不是為了給予每個人藥物而設計的。
也就是說,這是一個大新聞。藉由數百人經過許多年的努力,我們終於有了時間表,了解huntingtin降低藥物,RG6042,是否能用來治療HD並改善其症狀。
對於這個公布的訊息、huntingtin降低的領域更加的普遍,我們都很興奮。我們認為HD社群也會感到同樣的開心。請繼續關注HDBuzz,以了解更多其他試驗的進度。
Jeff Carroll博士的實驗室有跟Ionis製藥以及Wave Life Sciences公司有合作進行動物模型的研究。他跟這兩家公司並無人體試驗的相關財務利益。ED Wild博士是羅氏製藥研究的研究人員之一,同時也是先前Ionis研究的研究者。上述公司對於此報到並無任何干涉以及意見。
|


